É muito comum haver corrosão quando colocamos diferentes materiais
O amálgama dentário é constituído por uma mistura na qual o mercúrio combina-se com prata e estanho.
3 Hg22+ + 4 Ag (s) + 6 e-→ 2 Ag2Hg3(s) E°= +0,85V
2 Sn2+(aq) + 3 Ag (s) + 2 e-→ 1 Ag3Sn(s) E°= -0,05V
8 Sn2+(aq) + 1 Hg(s) + 16 e-→ 1 Sn8Hg(s) E°= -0,13V
Na realidade esse tipo de amalgama é constituído de 3 fases solidas formadas pelas seguintes substancias: Ag2Hg3, Ag3Sn, Sn8Hg.
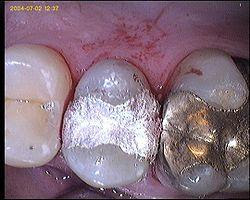
O problema surge quando um metal de maior potencial de redução (ouro, por exemplo) entra em contato co a obturação feita de amálgama. Nesse caso, se a obturação entra em contato com uma incrustação de ouro feita em um dente próximo, haverá corrosão na obturação. Isso acontece porque a obturação de amálgama atua como ânodo (menor potencial) e a incrustação de ouro como cátodo (maior potencial). Analisando os valores de E°, observa-se que o eletrodo Sn8Hg é o mais fácil de corroer. Quando isso ocorre, a liberação de íons Sn2+ na boca é responsável pelo desagradável sabor metálico. Por isso, um bom dentista jamais coloca um dente de ouro próximo a uma obturação de amálgama, por ser desconfortante para o paciente.
Referências bibliográficas
PERUZZO, Francisco Miragaia (Tito); Canto, Eduardo leite do. Química na abordagem do cotidiano. São Paulo: Moderna, 2006
. http://pt.wikipedia.org/wiki/Am%C3%A1lgama_de_prata
Nenhum comentário:
Postar um comentário